Регистрация медицинского изделия (МИ) — сложный и многоэтапный процесс, где каждая ошибка может стоить месяцев задержек и лишних затрат. Разбираем ключевые шаги, подводные камни и скрытые сроки
Содержание
- Общий процесс
- Шаг 1. Сбор документов — главный «пожиратель времени»
- Шаг 2. Технические испытания — «непредсказуемый» этап
- Шаг 3. Токсикологические испытания (если требуется)
- Шаг 4. Клинические испытания — самый предсказуемый этап
- Шаг 5. Формирование регистрационного досье
- Шаг 6. Получение РУ и внесение в реестр
- Выводы и рекомендации
Когда мы говорим о процессе получения регистрации мед изделия, лучше иметь его наглядную картинку
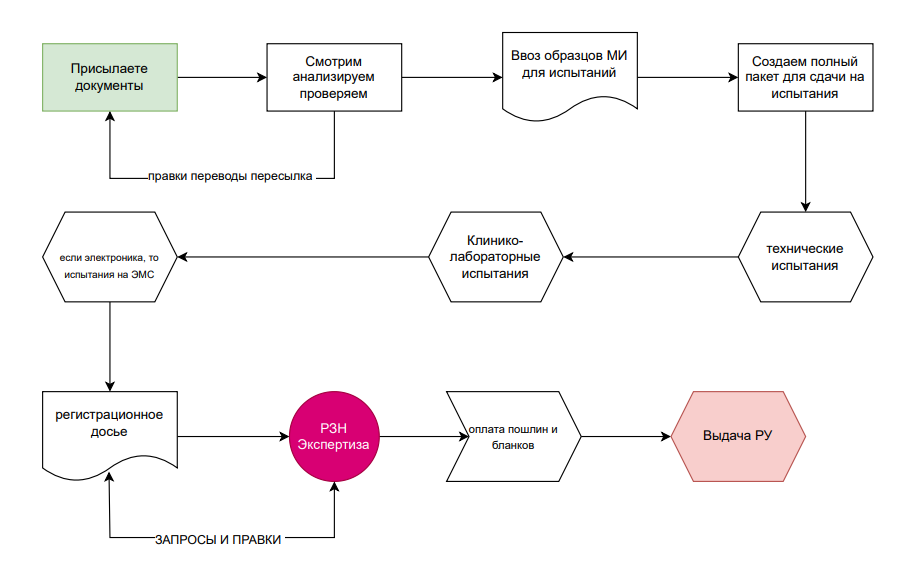
Схема получения Регистрационного удостоверения в Росздравнадзоре
Шаг 1. Сбор документов — главный «пожиратель времени»
Почему это самый сложный этап?
Несогласованность между сторонами:
- Производитель (площадка) может медлить с документами, директор не принял решение о бюджете, главный инженер не доделал документы, юристы не успели с доверенностью и пр. Кажется, что вот уже давно начали процесс регистрации в мыслях, а в реальности документов для старта не хватает. Возникает ощущение, что "мы уже долго возимся", а оно ложное. Отсчитывать старт регистрационного процесса стоит от полного набора документов.
- Регистратор требует доработок, а юр. отдел завода не успевает вносить правки.
- Процесс растягивается на месяцы из-за бесконечных уточнений. Очень часто профессионалы называют этот процесс главным пожирателем времени.
Запомните "золотой список" документов для старта регистрации?
✅ Техническая документация (ТУ, руководство по эксплуатации)
✅ Доказательства безопасности (отчеты, исследования)
✅ Информация о производителе (ISO, сертификаты GMP, доверенность на УПП)
Совет: Лучше сразу назначить ответственного за сбор документов с обеих сторон (производитель + регистратор). Иначе процесс провалится в «черную дыру» переписки». Лучше сделать еженедельную встречу с регистратором для обсуждения всех дел. Это значительно убыстрить процесс сбора документов. Еще отлично помогает наличие у регистратора шаблонов писем, запросов, схем для производственной площадки на трех языках: русском, китайском, английском.
Шаг 2. Технические испытания - «непредсказуемый» этап?
После подачи документов начинаются лабораторные испытания:
- Проверка на соответствие ГОСТам и техрегламентам.
- Анализ материалов, электробезопасности, биосовместимости.
Главная проблема: ❌ Стоимость и сроки неизвестны до последнего
- Испытательный центр определяет перечень ГОСТов только после изучения документации. А так как ее присылают не скоро, не сразу, то цену никто дать не может - это осложняет бюджетирование.
- Если производитель не предоставил полные данные — список испытаний может неожиданно расшириться.
Пример: Изделие заявлено как «стерильное» → нужно проверить по 5 ГОСТам. Но если в документации нет четкого описания метода стерилизации — испытаний станет больше, а цена вырастет».
Что делать?: заложить в бюджете больше денег, утвердить люфт по бюджету, добавить быть может лишние испытания, чтобы пройти эти процедуры с наименьшим риском, привлечь опытных регистраторов, которые уже делали подобный проект, чтобы оценить реакцию РЗН на набор испытаний - может, будет достаточно выбранных или по опыту нужно добавить. Почти в 100% случаях регистраторы действуют с наименьшим риском и у них есть опыт кейсов. Их помощь тут крайне желательна.
Кстати, найти регистратора с опытом проекта именно по вашему изделию можно в нашем каталоге. Выберите изделие и нажмите кнопку: Каталог регистраторов
Шаг 3. Токсикологические испытания (если требуется)
Проводятся для изделий, контактирующих с организмом (импланты, хирургические инструменты и т. д.).
Что проверяют?
- Отсутствие токсичных выделений.
- Биосовместимость (раздражающее действие, аллергенность).
Сложности:
- Нужен протокол испытаний, который согласовывается с экспертами.
- Если производитель не предоставил полные данные о материалах — испытания могут затянуться или подорожать.
Токсикологические испытания считаются самыми долгими. Ведь сами стандартны испытания требуют время для изготовления "вытяжек", анализа, их нельзя нарушать, а зачастую это 45-50 рабочих дней и эти сроки не подвинуть. Плюс ко всему, токсикологические лаборатории очень востребованы (к ним идут косметические производства и график испытаний может быть "забит" на полгода вперед), и их мало, поэтому встать в очередь на испытания - это целое испытание. Тут можно растерять время и деньги: ведь нужно быстро, а лаборатория за скорость возьмет наценку.
Что делать?
Смотри пункт 1: делать корректные документы, следить за составом, быть на связи с лабораторией, искать разные альтернативы. У нас на сайте есть полный каталог лабораторий, где вы можете найти лабораторию по ГОСТам и по ценам, сравнить отзывы и условия работы. Каталог по ссылке.
Шаг 4. Клинические испытания — самый предсказуемый этап, но есть нюанс
Проводятся в двух формах:
- На пациентах (для новых/сложных изделий).
- Бумажный аудит (если есть иностранные клинические данные).
Почему здесь меньше неожиданностей?
- Стоимость фиксированная (зависит от типа испытаний).
- Сроки четко регламентированы (обычно 1-2 месяца).
Но есть нюанс: Если изделие принципиально новое для РФ — Росздравнадзор может запросить дополнительные испытания с участием человека, что увеличит сроки и бюджет в десятки раз.
Что делать?
Запрашивать консультацию у опытных регистраторов, в сложных случаях у ВНИИМТ и НИКа (учреждения Росздравнадзора). Уточнять, есть ли точные аналоги вашего изделия в России. Или же регистратор может посоветовать другой код вида, под которым можно сделать регистрацию.
Шаг 5. Формирование регистрационного досье и сдача через Госуслуги
Когда все испытания пройдены:
- Регистратор собирает 30+ документов в единое досье.
- Подает в Росздравнадзор с доверенностью от производителя.
Что входит в досье?
- Протоколы испытаний.
- Заключения экспертов.
- Техническая и клиническая документация.
- Заявление на регистрацию.
Срок рассмотрения:
- Обычная процедура: до 50 рабочих дней
Какие риски могу быть?
Как правило, тут уже не может быть крупных "косяков". Если ваше регдосье проверил опытный консультант, то риск возвратов минимален. У всех он есть в районе 3-4%, но некоторые регистраторы даже предлагают бесплатные работы, если, вдруг, РЗН дал отказ на основании сданных документов. На этом этапе риск часто связан с работой платформы ГОСУСЛУГИ, куда надо загружать досье и ее стабильности. Огромный букет документов, сканов - все это нужно оцифровать и подписать электронной подписью. Если у вас нет в этом опыта - лучше довериться консультантам. Стоимость таких услуг около 30 000 рублей, но есть 100% гарантия.
Шаг 6. Получение РУ и внесение в реестр
Если Росздравнадзор одобрил досье:
✅ Выдается регистрационное удостоверение (РУ).
✅ Изделие вносится в Госреестр МИ.
Теперь можно:
- Легально ввозить и продавать изделие.
- Участвовать в госзакупках.
- Оформлять льготы по НДС.
Выводы
🔴 Главные риски и как их избежать
| Этап | Риски | Как минимизировать? |
|---|---|---|
| Сбор документов | Задержки из-за неполных данных | Назначить ответственного за согласование и описать четкий процесс |
| Технические испытания | Непредвиденные ГОСТы → рост цены | Заранее уточнить требования испытательного центра, найти больше альтернатив, найти варианты коллективной закупки испытаний |
| Клиника | Доп. требования РЗН | Использовать иностранные данные (если есть), запросить консультацию у регистраторов |
| Подача в РЗН | Ошибки в досье → возврат на доработку | Проверить всё через регистратора с опытом работы в с вашим изделием |
Вывод: Регистрация — это марафон, а не спринт
- 70% времени «съедает» подготовка документов и испытания.
- Бюджет может вырасти в 2 раза, если не учесть все ГОСТы.
- Лучший способ ускорить процесс — работать с опытным регистратором.
👉 Хотите заранее оценить сроки и бюджет? Выбирайте компанию-консультанта на сайте с максимально хорошими условиями и жмите на форму "прошу связаться со мной". Хороший консультант всегда первую консультацию проведет бесплатно.

